Le Butane: Gaz ou Liquide?
Quand je
secoue une bouteille de Butane, j'entends clapoter le liquide à l'intérieur.
Quand je regarde un briquet jetable, avec un modèle transparent, je vois un
liquide ayant l'aspect de l'eau à l'intérieur. Si j'appuie sur le petit levier,
sans faire d'étincelle, du gaz s'échappe avec un petit sifflement. Bon, faudrait
savoir, ce Butane est liquide ou gazeux?
Comme la
plupart des matériaux purs, il peut exister dans chacun des
trois états, suivant sa température ou sa
pression. Par exemple, pour le Butane justement, si la pression est celle du
niveau de la mer, il passe du liquide au gaz à tout près de 0°C... Dans la
bouteille, il est simplement assez comprimé, pour que les molécules très proches
les une des autres parviennent à s'accrocher faiblement: c'est alors un liquide.
Voyez aussi ce qui se passe pour l'Azote liquide.
Voici une
petite expérience spectaculaire à faire. , plutôt à l'air libre, sans trop de monde autour de soi et
avec des vêtements non inflammables...
Prenez une
petite bouteille de Butane de camping, retournez la, et ouvrez son robinet, son
bec au-dessus d'un tube à essais. Du gaz s'échappe alors, puis quelques gouttes
de liquide. Emplissez-en votre tube d'un demi centimètre.
 |
Après avoir ventilé
autour du tube, afin de chasser le gaz échappé, approchez une allumette
du sommet du tube. Le Butane donne une petite flamme orange. Le bord
du tube ne chauffe quasiment pas, étant sous la flamme. Le Butane liquide
du fond est en ébullition... à 0°C! le gaz monte, lentement, plus dense
que l'air, il est simplement aspiré par la flamme. Le bas du tube se
couvre de buée, la vapeur d'eau se condense sur cette paroi très froide,
et peut même givrer. |
 |
Notre bougie un peu
spéciale est même réglable. Il suffit de chauffer le fond dans le creux
de notre main: l'évaporation se fait alors plus intense, la flamme grandit.
La combustion est dite incomplète, les atomes de carbone du Butane forment
de petites particules de suie, qui brillent dans la flamme avec cette
couleur orange. Si la combustion était complète, tout le carbone se
combinerait au Dioxygène de l'air pour donner du Dioxyde de carbone,
invisible. La flamme serait bleue sombre, et très chaude. Observez la
jolie conduction de la lumière de la flamme, dans le liquide contenu
dans le tube.. |
Ceci dit, si le Butane est en ébullition à 0°C, pourquoi
l'eau bout-elle aussi tard, à 100°C?
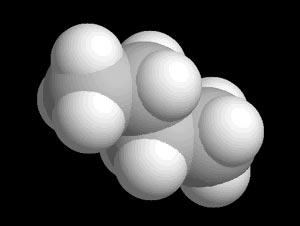 |
 |
| Une molécule de Butane (C4H10) |
Une molécule d'eau H2O |
En effet, les molécules d'eau sont beaucoup plus petites que celles de Butane,
on pourrait s'attendre à ce qu'il soit plus facile d'extraire de petites
molécules du liquide que de plus grosses, non?
|
En fait, les atomes d'Oxygène aiment plus les électrons que ceux de
Carbone. Ils ont ainsi tendance à tirer à eux les électrons de la liaison
entre eux et les Hydrogènes. Ce qui change tout! La molécule d'eau devient
alors polarisée, avec un côté (Oxygène) négatif, et des côtés (Hydrogènes)
positifs. Elles forment alors, dans l'eau liquide des liaisons
électriques, comme si elles se donnaient la main... |
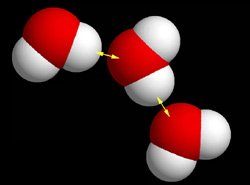 |
Les molécules d'eau sont ainsi assez difficile à séparer les une des autres,
pour les faire passer à l'état gazeux: cela demande beaucoup plus d'énergie
que pour le Butane, qui lui est déjà gazeux à beaucoup plus basse température.
C'est une chance pour la Terre que l'eau, ce liquide si vital, soit aussi
difficile à évaporer.




