La surfusion? Qu'est-ce?
Quand on refroidit de l'eau,
depuis tout petit, on apprend qu'un glaçon se forme à 0°C. Du moins si l'on est
à la pression atmosphérique normale, mais ça, on l'apprend un peu plus tard...
Par contre, il est possible
d'avoir de l'eau liquide à des températures négatives, sans toucher à la
pression. Curieux, mais pas si difficile que ça à visualiser. Voici une petite
expérience que vous pouvez faire:
Achetez une bouteille d'eau
déminéralisée (de l'eau distillée vendue pour les fers à repasser, elle est très
pure, du moins, plus que celle du robinet...). Mettez-en quelques millilitres
dans un tube à essais, un thermomètre planté dedans. L'ensemble est immergé dans
un mélange de glace et de sel (qui peut
descendre facilement à -10°C). Surveillez la température. Vous risquez fort,
si vous ne touchez pas au thermomètre, de voir la température intérieure du tube
chuter régulièrement, plus bas que 0°C. Si vous tentez alors de bouger le
thermomètre, vous le sentirez se mouvoir librement (l'eau est encore liquide),
puis se figer brutalement (l'eau prend en masse). Attention alors à ne pas le
casser... La température sera remontée à 0°C, puis reprendra sa descente
régulière. Bizarre non?
 |
 |
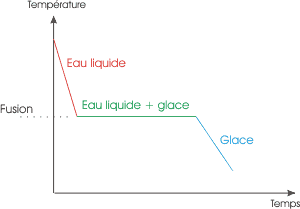
| Voilà ce qui se passe lors
d'une solidification "classique" (ou fusion si on lit le graphique
dans l'autre sens) . Lors de du passage liquide > solide, la température
reste à 0°C tant que tout le liquide n'est pas solidifié. C'est un palier
de température, qui a lieu lors du changement d'état. |
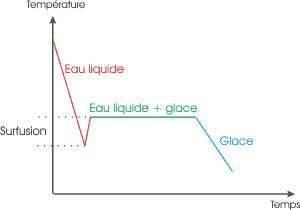
Lors d'une surfusion, l'eau
reste liquide en dessous de 0°C, mais, à la moindre perturbation, remonte
à sa température classique de changement d'état. |
En fait, les impuretés contenues
dans l'eau facilitent sa congélation. C'est un peu le même phénomène qui donne
naissance aux bulles dans un verre de
champagne, ou qui fait croître les
flocons de neige. Des vibrations ou des secousses peuvent également
favoriser la solidification. On comprend alors qu'un petit volume d'eau très
pure soit favorable à une surfusion s'il n'y a aucune perturbation.
Le phénomène peut-être rendu
encore plus marquant si l'on voit la congélation instantanée se produire. Ce
n'est pas vraiment possible avec un tube à essais enfoncé dans un mélange
réfrigérant. Mais ça le devient si vous vous enfermez dans le congélateur avec
votre tube à portée d'oeil... Pas tenté? Essayez alors avec une webcam dans le
frigo! regardez ce que cela donne.
 |
 |
 |
| Là, il fait encore "chaud",
3°C, l'eau est bien sûr liquide. |
Surfusion! Il fait -5°C, l'eau
est toujours liquide!... |
Quelques secondes plus tard,
l'eau s'est figée brutalement, la température est remontée à 0°C, puis
est redescendue plus lentement, il fait -1°C ici... |
Vous
pouvez voir le petit film
correspondant (346 ko), ou l'on voit la congélation de l'eau se faire en
masse...
A ce propos, il est une petite histoire,
écrite par Malaparte (dans "Kaput"), que je vous résume rapidement:
Dans les années 40, en hiver, une troupe de chevaux affolés par un incendie
plonge dans les eaux de l'immense lac Ladoga, en Russie, près de la frontière
Finnoise. Une fois entrés dans l'eau, celle-ci se congèle brutalement, emprisonnant
les malheureux animaux... Cela ressemble bien à une solidification après une
phase de surfusion. Mais il est quand même étonnant d'imaginer ce lac aussi
pur et calme que ce qui est habituellement nécessaire de réunir comme conditions.
Les chevaux ne se seraient-ils pas plutôt aventurés sur une glace trop fragile
pour eux?...
Un correspondant, Grégoire, m'a envoyé de Russie cet
hiver un saisissant petit film: il fait -30°C dans un placard en équilibre
avec la température extérieure. Dans ce placard, une bouteille
d'eau minérale: liquide... Avec quelques chocs, elle fige à
grande vitesse. Voyez
ce film ici (1,16 Mo).
|
 |
Ceci dit, on peut atteindre pas
loin de -40°C avec de l'eau surfondue, dans d'excellents conditions! Quel sera
votre record?
Pour finir, un moyen de reconstituer ce phénomène de surfusion,
de manière assez fiable et reproductible. On sera ici dans un cas assez
particulier de recristallisation: l'acétate de sodium (ou éthanoate
de sodium) est très soluble dans l'eau. Si vous en fabriquez une solution
quasiment saturée à haute température, lorsqu'elle refroidira,
vous aurez un liquide limpide et incolore. Or, à température ambiante,
cette solution devrait être solide, elle est en état de surfusion.
Il suffit d'ajouter un petit cristal d'acetate de sodium, et la solution passe
rapidement à l'état solide. Et comme ce changement d'état
à lieu normalement vers 50°C, le matériau se réchauffe
à cette température pour passer à l'état solide.
Cette curieuse transformation est utilisée pour faire des "chaufferettes":
des poches de cette solution, que l'on fait passer à l'état solide
en triturant une petite lamelle métallique noyée dans le mélange.
Ces cisaillements auront localement l'énergie suffisante pour faire démarrer
la croissance des germes, et le passage à l'état solide s'accompagnera
d'un dégagement de chaleur. Le processus est réversible: une fois
solide, on le repasse à l'état liquide au bain-marie, puis on
le laisse refroidir sans le secouer, et il est alors près à relibérer
son énergie... Et en plus, c'est joli à regarder!...

Petite video (680k0, en DivX)






